أثناء تفاعل البلمرة المتسلسل (PCR)، غالباً ما يتم مواجهة بعض العوامل المتداخلة.
نظراً للحساسية العالية جداً لتقنية تفاعل البوليميراز المتسلسل (PCR)، يعتبر التلوث أحد أهم العوامل التي تؤثر على نتائج تفاعل البوليميراز المتسلسل ويمكن أن ينتج عنه نتائج إيجابية خاطئة.
لا تقل أهمية عن ذلك المصادر المختلفة التي تؤدي إلى نتائج سلبية خاطئة. فإذا تم تثبيط أو إعاقة جزء أو أكثر من المكونات الأساسية لمزيج تفاعل البوليميراز المتسلسل (PCR) أو تفاعل التضخيم نفسه، فقد يتعطل الفحص التشخيصي. وهذا بدوره قد يؤدي إلى انخفاض الكفاءة، بل وحتى إلى نتائج سلبية خاطئة.
إضافةً إلى التثبيط، قد يحدث فقدان لسلامة الحمض النووي المستهدف نتيجةً لظروف الشحن و/أو التخزين قبل تحضير العينة. وعلى وجه الخصوص، قد تؤدي درجات الحرارة المرتفعة أو التخزين غير المناسب إلى تلف الخلايا والأحماض النووية. يُعد تثبيت الخلايا والأنسجة وتضمينها في البارافين من الأسباب المعروفة لتفتت الحمض النووي، وهي مشكلة مستمرة (انظر الشكلين 1 و2). في هذه الحالات، حتى أفضل عمليات العزل والتنقية لن تُجدي نفعًا.
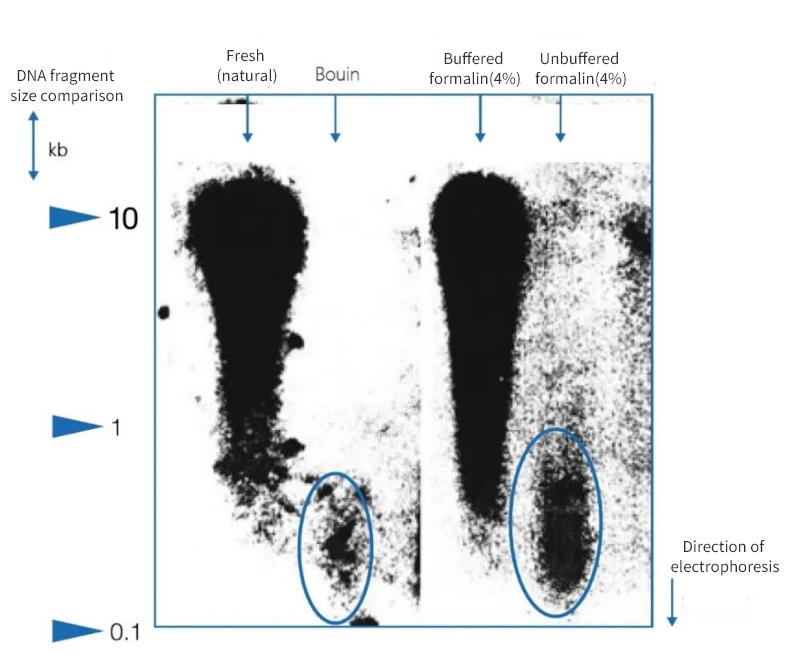
الشكل 1 | تأثير التثبيت على سلامة الحمض النووي
أظهر الفصل الكهربائي على هلام الأغاروز أن جودة الحمض النووي المستخلص من مقاطع البارافين في عينات التشريح تختلف اختلافًا كبيرًا. وُجد الحمض النووي بأطوال شظايا متوسطة مختلفة في المستخلصات تبعًا لطريقة التثبيت. لم يُحفظ الحمض النووي إلا عند تثبيته في عينات مجمدة طبيعية وفي الفورمالين المتعادل المخفف. أدى استخدام مُثبِّت بوين شديد الحموضة أو الفورمالين غير المخفف المحتوي على حمض الفورميك إلى فقدان كبير للحمض النووي، حيث يكون الجزء المتبقي شديد التجزئة.
على اليسار، يتم التعبير عن طول الأجزاء بوحدات الكيلوبايت (kbp).
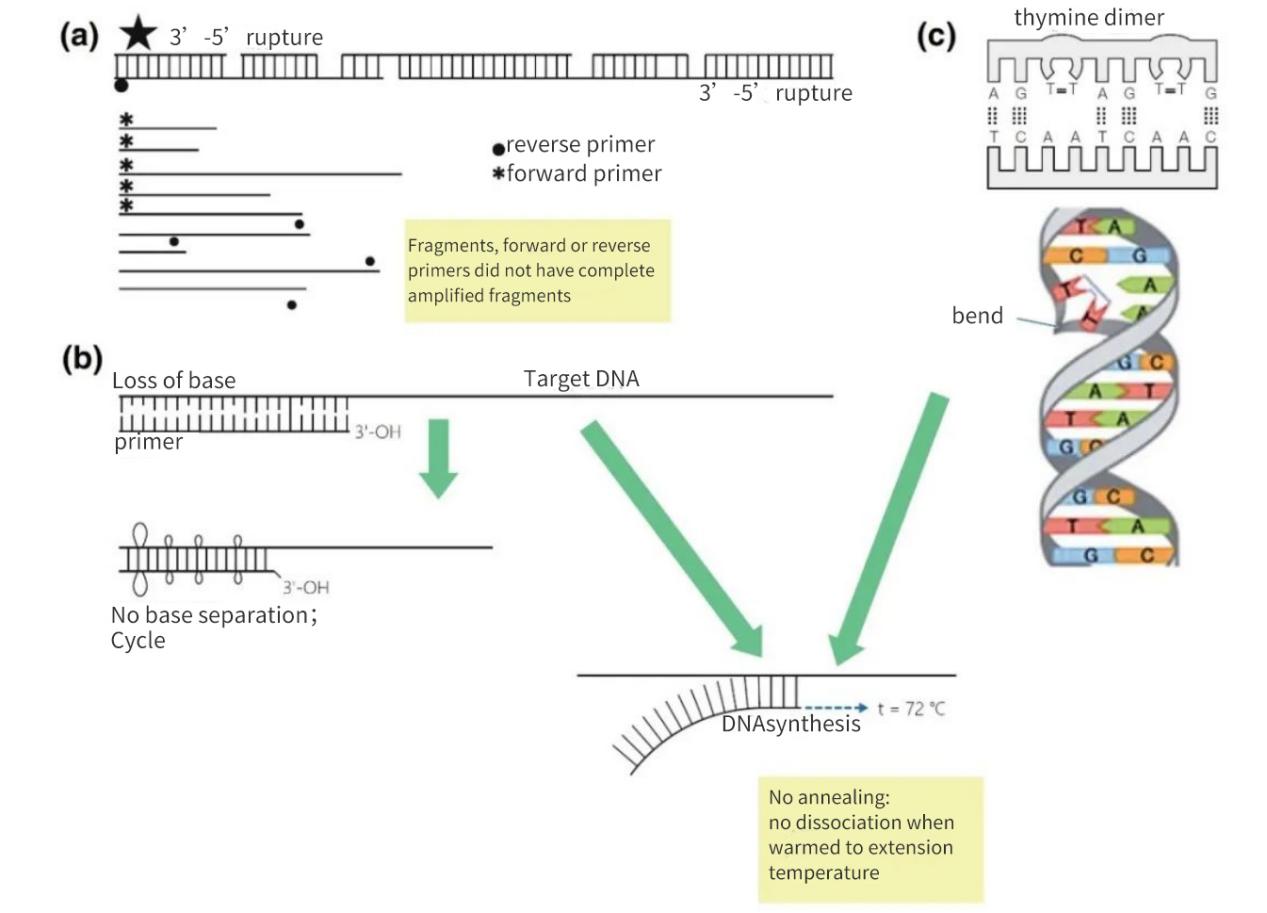
الشكل 2 | فقدان سلامة أهداف الحمض النووي
(أ) سيؤدي وجود فجوة بين طرفي السلسلة 3′ و5′ على كلا الشريطين إلى انقطاع في الحمض النووي المستهدف. سيستمر تخليق الحمض النووي على الجزء الصغير. مع ذلك، إذا كان موقع ارتباط البادئ مفقودًا على جزء الحمض النووي، فلن يحدث سوى تضخيم خطي. في أفضل الأحوال، قد تتشبع الأجزاء ببعضها البعض، لكن ستكون الكمية الناتجة ضئيلة وأقل من مستوى الكشف.
(ب) يؤدي فقدان القواعد، ويرجع ذلك أساسًا إلى إزالة البيورين وتكوين ثنائي الثيميدين، إلى انخفاض في عدد الروابط الهيدروجينية وانخفاض في درجة حرارة الانصهار. خلال مرحلة التسخين المطولة، ستنفصل البادئات عن الحمض النووي الأساسي ولن تلتصق حتى في ظل ظروف أقل صرامة.
(ج) تشكل قواعد الثايمين المتجاورة ثنائي TT.
من المشاكل الشائعة الأخرى في التشخيص الجزيئي عدم كفاية استخلاص الأحماض النووية المستهدفة مقارنةً باستخلاص الفينول-الكلوروفورم. في الحالات القصوى، قد يؤدي ذلك إلى نتائج سلبية خاطئة. يمكن توفير الكثير من الوقت عن طريق غلي حطام الخلايا أو هضمه إنزيميًا، لكن هذه الطريقة غالبًا ما تُنتج حساسية منخفضة لتفاعل البوليميراز المتسلسل (PCR) بسبب عدم كفاية استخلاص الأحماض النووية.
تثبيط نشاط البوليميراز أثناء التضخيم
بشكل عام، يُستخدم مصطلح التثبيط كمفهوم شامل لوصف جميع العوامل التي تؤدي إلى نتائج غير مثالية في تفاعل البوليميراز المتسلسل (PCR). من الناحية الكيميائية الحيوية البحتة، يقتصر التثبيط على نشاط الإنزيم، أي أنه يقلل أو يمنع تحويل الركيزة إلى ناتج من خلال التفاعل مع الموقع النشط لإنزيم بوليميراز الحمض النووي أو العامل المساعد له (مثل أيونات المغنيسيوم لإنزيم بوليميراز الحمض النووي Taq).
يمكن للمكونات الموجودة في العينة أو المحاليل المنظمة والمستخلصات المختلفة التي تحتوي على الكواشف أن تثبط الإنزيم بشكل مباشر أو تحبس عوامله المساعدة (مثل EDTA)، مما يؤدي إلى تعطيل البوليميراز وبالتالي انخفاض نتائج تفاعل البوليميراز المتسلسل أو نتائج سلبية خاطئة.
مع ذلك، تُصنّف العديد من التفاعلات بين مكونات التفاعل والأحماض النووية الحاملة للهدف ضمن "مثبطات تفاعل البوليميراز المتسلسل". فعندما تُعطّل سلامة الخلية نتيجةً للعزل، ويتحرر الحمض النووي، قد تحدث تفاعلات بين العينة ومحلولها المحيط والطور الصلب. على سبيل المثال، يمكن لـ"الكاسحات" أن ترتبط بالحمض النووي أحادي أو ثنائي السلسلة عبر تفاعلات غير تساهمية، مما يعيق عملية العزل والتنقية عن طريق تقليل عدد الأهداف التي تصل في النهاية إلى وعاء تفاعل البوليميراز المتسلسل.
بشكل عام، توجد مثبطات تفاعل البوليميراز المتسلسل في معظم سوائل الجسم والكواشف المستخدمة في الاختبارات التشخيصية السريرية (اليوريا في البول، والهيموجلوبين والهيبارين في الدم)، والمكملات الغذائية (المكونات العضوية، والجليكوجين، والدهون، وأيونات الكالسيوم) والمكونات الموجودة في البيئة (الفينولات، والمعادن الثقيلة).
| المثبطات | مصدر |
| أيونات الكالسيوم | الحليب، نسيج العظام |
| الكولاجين | منديل |
| أملاح الصفراء | براز |
| الهيموجلوبين | في الدم |
| الهيموجلوبين | عينات الدم |
| حمض الهيوميك | التربة، النبات |
| دم | دم |
| اللاكتوفيرين | دم |
| الميلانين (الأوروبي) | الجلد والشعر |
| الميوغلوبين | النسيج العضلي |
| السكريات المتعددة | نبات، براز |
| بروتياز | لبن |
| اليوريا | البول |
| عديد السكاريد المخاطي | الغضروف، الأغشية المخاطية |
| اللجنين، السليلوز | النباتات |
توجد مثبطات تفاعل البوليميراز المتسلسل (PCR) الأكثر شيوعًا في البكتيريا والخلايا حقيقية النواة، والحمض النووي غير المستهدف، والجزيئات الكبيرة المرتبطة بالحمض النووي في مصفوفات الأنسجة، والمعدات المختبرية مثل القفازات والبلاستيك. ويُعد تنقية الأحماض النووية أثناء الاستخلاص أو بعده الطريقة المُفضلة لإزالة مثبطات تفاعل البوليميراز المتسلسل.
اليوم، يمكن للعديد من أجهزة الاستخلاص الآلية أن تحل محل العديد من البروتوكولات اليدوية، ولكن لم يتم تحقيق استخلاص أو تنقية كاملة للأهداف. قد تظل بعض المثبطات موجودة في الأحماض النووية المنقاة أو ربما تكون قد بدأت بالفعل في التأثير. توجد استراتيجيات مختلفة للحد من تأثير هذه المثبطات. يُمكن أن يكون لاختيار البوليميراز المناسب تأثير كبير على فعالية المثبطات. من الطرق الأخرى المُثبتة للحد من تثبيط تفاعل البوليميراز المتسلسل (PCR) زيادة تركيز البوليميراز أو إضافة مواد مثل ألبومين المصل البقري (BSA).
يمكن إثبات تثبيط تفاعلات PCR باستخدام مراقبة جودة العملية الداخلية (IPC).
يجب الحرص على إزالة جميع الكواشف والمحاليل الأخرى الموجودة في مجموعة الاستخلاص، مثل الإيثانول، وEDTA، وCETAB، وLiCl، وGuSCN، وSDS، والإيزوبروبانول، والفينول، من الحمض النووي المعزول عن طريق غسله جيدًا. فقد تُنشّط هذه المواد تفاعل البلمرة المتسلسل (PCR) أو تُثبّطه، وذلك تبعًا لتركيزها.
تاريخ النشر: 19 مايو 2023
 中文网站
中文网站