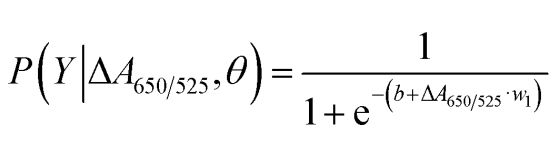يُعدّ الكشف المبكر عن السرطان باستخدام الخزعة السائلة اتجاهاً جديداً في مجال الكشف عن السرطان وتشخيصه، اقترحه المعهد الوطني الأمريكي للسرطان في السنوات الأخيرة، بهدف الكشف عن السرطان في مراحله المبكرة أو حتى الآفات ما قبل السرطانية. وقد استُخدمت هذه التقنية على نطاق واسع كعلامة حيوية جديدة للتشخيص المبكر لأنواع مختلفة من الأورام الخبيثة، بما في ذلك سرطان الرئة، وأورام الجهاز الهضمي، والأورام الدبقية، وأورام الجهاز التناسلي الأنثوي.
إن ظهور منصات لتحديد المؤشرات الحيوية لمشهد الميثيل (Methylscape) لديه القدرة على تحسين الفحص المبكر الحالي للسرطان بشكل كبير، مما يضع المرضى في المرحلة المبكرة القابلة للعلاج.
طوّر باحثون مؤخراً منصة استشعار بسيطة ومباشرة للكشف عن التغيرات في مواقع مثيلة الحمض النووي، تعتمد على جسيمات نانوية ذهبية مغلفة بالسيستامين (Cyst/AuNPs) مقترنة بمستشعر حيوي يعمل بالهواتف الذكية، مما يتيح الكشف المبكر السريع عن مجموعة واسعة من الأورام. ويمكن إجراء الكشف المبكر عن سرطان الدم (اللوكيميا) في غضون 15 دقيقة من استخلاص الحمض النووي من عينة الدم، بدقة تصل إلى 90%. عنوان المقال: الكشف السريع عن الحمض النووي للسرطان في دم الإنسان باستخدام جسيمات نانوية ذهبية مغلفة بالسيستامين وهاتف ذكي مزود بتقنية التعلم الآلي.
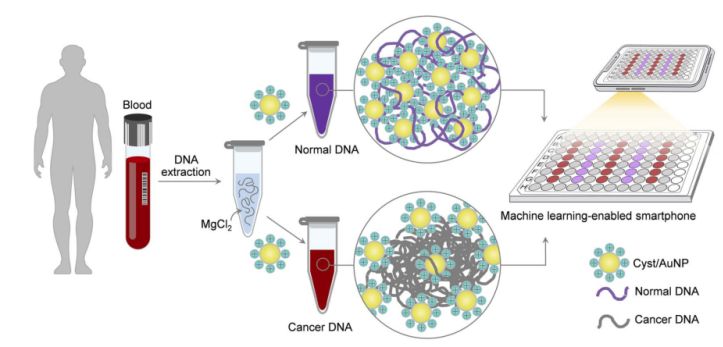
الشكل 1. يمكن إنجاز منصة استشعار بسيطة وسريعة لفحص السرطان عبر مكونات Cyst/AuNPs في خطوتين بسيطتين.
يوضح الشكل 1 هذه العملية. في البداية، استُخدم محلول مائي لإذابة شظايا الحمض النووي. ثم أُضيفت جزيئات الذهب النانوية المُغطاة بالسيستين (Cyst/AuNPs) إلى المحلول. يتميز الحمض النووي الطبيعي والسرطاني بخصائص مثيلة مختلفة، مما ينتج عنه شظايا حمض نووي ذات أنماط تجميع ذاتي مختلفة. يتجمع الحمض النووي الطبيعي بشكل غير مُحكم، وفي النهاية يُكوّن تجمعات من جزيئات الذهب النانوية المُغطاة بالسيستين، مما يؤدي إلى انزياح لونها نحو الأحمر، بحيث يمكن ملاحظة تغير اللون من الأحمر إلى البنفسجي بالعين المجردة. في المقابل، يؤدي نمط المثيلة الفريد للحمض النووي السرطاني إلى إنتاج تجمعات أكبر من شظايا الحمض النووي.
تم التقاط صور لألواح 96 بئراً باستخدام كاميرا هاتف ذكي. تم قياس الحمض النووي للسرطان بواسطة هاتف ذكي مزود بتقنية التعلم الآلي مقارنةً بالطرق القائمة على التحليل الطيفي.
فحص السرطان في عينات الدم الحقيقية
لتعزيز فعالية منصة الاستشعار، استخدم الباحثون مستشعرًا نجح في التمييز بين الحمض النووي الطبيعي والسرطاني في عينات دم حقيقية. تُنظّم أنماط مثيلة الحمض النووي في مواقع CpG التعبير الجيني فوق الجيني. وقد لوحظ تناوب التغيرات في مثيلة الحمض النووي، وبالتالي في التعبير عن الجينات التي تُعزز تكوّن الأورام، في جميع أنواع السرطان تقريبًا.
استخدم الباحثون، كنموذج لأنواع السرطان الأخرى المرتبطة بمثيلة الحمض النووي، عينات دم من مرضى اللوكيميا وأفراد أصحاء لدراسة فعالية نمط المثيلة في التمييز بين أنواع سرطان الدم. لا يتفوق هذا المؤشر الحيوي لنمط المثيلة على طرق الفحص السريع الحالية للوكيميا فحسب، بل يُظهر أيضًا إمكانية توسيع نطاق استخدامه ليشمل الكشف المبكر عن مجموعة واسعة من أنواع السرطان باستخدام هذا التحليل البسيط والمباشر.
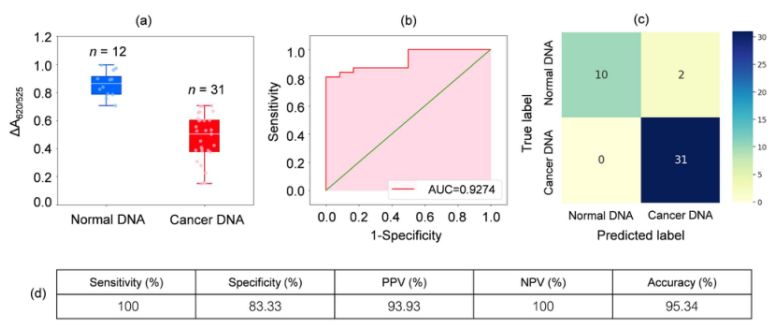
تم تحليل الحمض النووي المستخلص من عينات دم مأخوذة من 31 مريضًا بسرطان الدم و12 شخصًا سليمًا. وكما هو موضح في مخطط الصندوق في الشكل 2أ، كان الامتصاص النسبي لعينات السرطان (ΔA650/525) أقل من امتصاص الحمض النووي المستخلص من العينات الطبيعية. ويعود ذلك أساسًا إلى زيادة كراهية الماء، مما أدى إلى تكتل كثيف للحمض النووي السرطاني، الأمر الذي منع تكتل جسيمات السيستين/الذهب النانوية. ونتيجة لذلك، تشتتت هذه الجسيمات النانوية تمامًا في الطبقات الخارجية لتجمعات الخلايا السرطانية، مما أدى إلى اختلاف تشتت جسيمات السيستين/الذهب النانوية الممتصة على تجمعات الحمض النووي الطبيعية والسرطانية. ثم تم إنشاء منحنيات ROC بتغيير العتبة من قيمة دنيا لـ ΔA650/525 إلى قيمة قصوى.
الشكل 2. (أ) قيم الامتصاص النسبي لمحاليل الكيس/جسيمات الذهب النانوية، موضحًا وجود الحمض النووي الطبيعي (الأزرق) والسرطاني (الأحمر) في ظل الظروف المُحسَّنة.
(DA650/525) من مخططات الصندوق؛ (ب) تحليل منحنى ROC وتقييم الاختبارات التشخيصية. (ج) مصفوفة الارتباك لتشخيص المرضى الأصحاء ومرضى السرطان. (د) حساسية، وخصوصية، وقيمة التنبؤ الإيجابية (PPV)، وقيمة التنبؤ السلبية (NPV)، ودقة الطريقة المطورة.
كما هو موضح في الشكل 2ب، أظهرت المساحة تحت منحنى ROC (AUC = 0.9274) التي تم الحصول عليها للمستشعر المُطوَّر حساسيةً ونوعيةً عاليتين. وكما يتضح من مخطط الصندوق، فإن أدنى نقطة تمثل مجموعة الحمض النووي الطبيعي لا تنفصل بوضوح عن أعلى نقطة تمثل مجموعة الحمض النووي السرطاني؛ لذلك، تم استخدام الانحدار اللوجستي للتمييز بين المجموعتين الطبيعية والسرطانية. وبمعرفة مجموعة من المتغيرات المستقلة، يُقدِّر الانحدار اللوجستي احتمالية وقوع حدث ما، مثل مجموعة سرطانية أو طبيعية. يتراوح المتغير التابع بين 0 و1، وبالتالي فإن النتيجة هي احتمال. وقد حددنا احتمالية تحديد السرطان (P) بناءً على ΔA650/525 كما يلي.
حيث b=5.3533 و w1=-6.965. في تصنيف العينات، يشير احتمال أقل من 0.5 إلى عينة طبيعية، بينما يشير احتمال 0.5 أو أعلى إلى عينة سرطانية. يوضح الشكل 2ج مصفوفة الارتباك الناتجة عن التحقق المتقاطع "تركها دون تغيير"، والتي استُخدمت للتحقق من استقرار طريقة التصنيف. يلخص الشكل 2د تقييم الاختبار التشخيصي للطريقة، بما في ذلك الحساسية والنوعية والقيمة التنبؤية الإيجابية (PPV) والقيمة التنبؤية السلبية (NPV).
أجهزة الاستشعار الحيوية القائمة على الهواتف الذكية
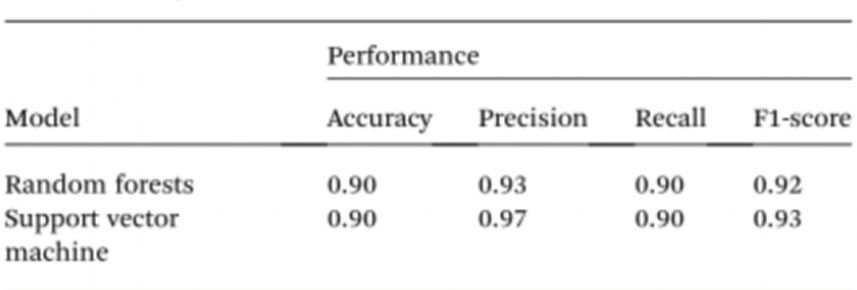
لتبسيط اختبار العينات دون الحاجة إلى أجهزة قياس الطيف الضوئي، استخدم الباحثون الذكاء الاصطناعي لتفسير لون المحلول والتمييز بين الأفراد الأصحاء والمصابين بالسرطان. وبناءً على ذلك، استُخدمت تقنية رؤية الحاسوب لتحويل لون محلول السيست/جسيمات الذهب النانوية إلى حمض نووي طبيعي (بنفسجي) أو حمض نووي سرطاني (أحمر) باستخدام صور لألواح 96 بئرًا مُلتقطة بكاميرا الهاتف المحمول. يُمكن للذكاء الاصطناعي خفض التكاليف وتحسين سهولة تفسير لون محاليل الجسيمات النانوية، دون الحاجة إلى أي ملحقات بصرية للهواتف الذكية. وأخيرًا، تم تدريب نموذجين للتعلم الآلي، وهما نموذج الغابة العشوائية (RF) ونموذج آلة المتجهات الداعمة (SVM)، لبناء النماذج. وقد صنّف كلا النموذجين العينات بشكل صحيح على أنها إيجابية وسلبية بدقة بلغت 90%. يشير هذا إلى إمكانية استخدام الذكاء الاصطناعي في الاستشعار الحيوي عبر الهواتف المحمولة.
الشكل 3. (أ) الفئة المستهدفة للمحلول المسجلة أثناء تحضير العينة لخطوة التقاط الصورة. (ب) صورة نموذجية ملتقطة أثناء خطوة التقاط الصورة. (ج) شدة لون محلول الكيس/جسيمات الذهب النانوية في كل بئر من آبار صفيحة الـ 96 بئراً، مستخرجة من الصورة (ب).
باستخدام جسيمات الذهب النانوية المغلفة بالسيستين (Cyst/AuNPs)، نجح الباحثون في تطوير منصة استشعار بسيطة للكشف عن تغيرات مثيلة الحمض النووي، بالإضافة إلى مستشعر قادر على التمييز بين الحمض النووي الطبيعي والحمض النووي السرطاني عند استخدام عينات دم حقيقية لفحص سرطان الدم. وقد أظهر المستشعر المُطور قدرة الحمض النووي المستخلص من عينات الدم الحقيقية على الكشف السريع والفعال من حيث التكلفة عن كميات ضئيلة من الحمض النووي السرطاني (3 نانومتر) لدى مرضى سرطان الدم في غضون 15 دقيقة، وبدقة بلغت 95.3%. ولتبسيط عملية فحص العينات بشكل أكبر، من خلال الاستغناء عن استخدام مطياف ضوئي، تم استخدام تقنية التعلم الآلي لتفسير لون المحلول والتمييز بين الأفراد الأصحاء والمصابين بالسرطان باستخدام صورة ملتقطة بهاتف محمول، وقد تحققت دقة مماثلة بلغت 90.0%.
المرجع: DOI: 10.1039/d2ra05725e
تاريخ النشر: 18 فبراير 2023
 中文网站
中文网站